15 novembre 2022 | Atelier Theia
Télédétection et Risques & Maladies Infectieuses
Toutes les présentations

4 octobre 2022 | Atelier Theia

12 octobre 2021 | Atelier Theia
Les utilisations de la télédétection pour la qualité des eaux continentales et aux interfaces
Enjeux sociétaux

Le thème « Santé et bien-être » fait partie des dix grands défis sociétaux actuels identifiés par la nouvelle Stratégie Nationale de Recherche du Ministère de l’Enseignement et de la recherche, en lien étroit avec le programme européen de recherche et d’innovation Horizon 2020. La santé est en effet un facteur de développement stratégique, tant par l’activité économique qui lui est liée que par les attentes de chacun des citoyens pour une maitrise des risques sanitaires, condition du bien-être et de l’épanouissement personnel. Par ailleurs, les enjeux économiques de la santé animale et végétale sont considérables. Ainsi, l’enjeu pour la recherche est de contribuer à mieux prévenir, dépister et traiter les pathologies qui pèsent sur la santé humaine, animale ou végétale.

Parmi celles-ci, les maladies infectieuses, causées par un micro-organisme pathogène (virus, bactérie, parasite, champignon), restent une des premières causes de mortalité dans le monde, responsables de près d’un tiers des décès dans les pays à revenu faible (Organisation Mondiale de la Santé). L’acquisition des agents pathogènes responsables de ces maladies peut se faire par contact direct avec un réservoir infecté comme l’eau (ex. choléra, bilharziose,…), par contact direct avec un hôte comme l’homme (ex. méningite), ou encore par la piqûre d’un insecte vecteur (ex. paludisme, dengue, chickungunya, leishmanioses, fièvre de la Vallée du Rift, maladie de Lyme, fièvre du Nil Occidental …). La lutte contre ces maladies, associant veille épidémiologique, développement de traitements et de vaccins, reste par conséquent plus que jamais d’actualité dans un contexte de changements environnementaux rapides (changement climatique, croissance démographique, déforestation et urbanisation, intensification de l’agriculture, mondialisation et intensification des échanges,…) qui favorisent le maintien et la dispersion des pathogènes et contribuent ainsi aux caractères endémiques ou émergents de maladies chez l’Homme, la faune sauvage ou domestique et les plantes. D’autre part, les maladies non transmissibles (maladies respiratoires, maladies cardio-vasculaires, cancers,..) sont responsables d’un nombre croissant de décès dans le monde (Organisation Mondiale de la Santé), et peuvent avoir pour cause des éléments organiques ou inorganiques présents dans l’environnement (ex. pollution atmosphérique, accentuée par le changement climatique et la densification de population dans les centres urbains ; méthylmercure dans les eaux de rivière, naturellement présent dans certaines régions du monde, mais dont la concentration peut être augmentée par la déforestation et certains procédés liés à l’orpaillage …).
Face à ces enjeux sociétaux, une recherche intégrée pour étudier les liens étroits et complexes qui existent entre l’environnement, les écosystèmes et les agents étiologiques responsables de maladies dans les populations humaines, animales et végétales, se développe, notamment autour des concepts de ‘One Health’ (une santé) et ‘EcoHealth’ (santé environnementale). Ces études nécessitent la compréhension des mécanismes en jeu et l’identification des facteurs favorables à l’émergence, à la propagation et à la persistance des pathologies. Ces facteurs peuvent être environnementaux, climatiques, démographiques, socio-économiques ou comportementaux. Certains de ces facteurs peuvent, ou pourraient, être identifiés depuis l’Espace, ce qui nécessite le développement de méthodes performantes pour faire de la télédétection un outil adapté pour la caractérisation, la cartographie et le suivi de ces facteurs de risque : c’est le défi de la thématique « Télédétection et santé ».
Question de recherche
Les questions de recherche liées à la thématique « télédétection et santé » concernent l’ensemble de la chaîne de traitement de l’information, de l’acquisition de la donnée jusqu’aux actions de prévention et de contrôle des maladies. Elles se déclinent en trois grandes familles :
1) Comment caractériser les situations et phénomènes pertinents pour l’étude des éco-pathosystèmes et la gestion de la santé ? Depuis les premières utilisations de la télédétection dans le domaine de la santé dans les années 70, la communauté scientifique a acquis un certain recul sur la caractérisation des conditions environnementales favorables à la transmission ou à la propagation de maladies à déterminants environnementaux, par l’identification directe de la présence d’agents pathogènes (particules atmosphériques par exemple) ou la caractérisation des conditions favorables à la présence des vecteurs, des réservoirs sauvages, des populations d’hôtes sensibles (humaines, animales ou végétales) et de leurs interactions. Cependant, des efforts de recherche demeurent nécessaires afin d’assurer une plus grande objectivité dans le choix des paramètres à caractériser et dans leur mode de caractérisation, d’autant plus que les progrès technologiques permettant l’accès à des résolutions spatiales et temporelles de plus en plus importantes demandent de reconsidérer sans cesse ces questions de recherche. Les questions spécifiques sont donc :
- Quels sont les capteurs et les méthodes de traitement d’image, de changement d’échelle, d’intégration de données multi-sources, les mieux adaptés ? En particulier quels sont les produits satellitaires environnementaux (par exemple température, humidité, aérosols, surface, etc) les plus pertinents ?
- Comment caractériser et suivre l’évolution spatio-temporelle des déterminants favorables à l’émergence et propagation des maladies en s’appuyant sur la télédétection ?
- Comment caractériser, par télédétection, la distribution spatiale des situations socio-démographiques et comportementales permettant d’identifier et de caractériser les populations les plus vulnérables ? Si la très haute résolution spatiale semble pertinente dans ce cas, en permettant de caractériser finement les modes d’occupation humaine des territoires étudiés, les travaux restent peu nombreux sur cette question.
2) Comment analyser conjointement des données complexes (multi-sources, multi-résolution, multi-échelles, quantitatives, qualitatives, imprécises voir incertaines, aux supports temporel et spatial différents, etc.), pour :
- la description des processus (de transmission, de diffusion) et leur explication ?
- la modélisation, afin de permettre :
- la construction d’indicateurs environnementaux pertinents et sensibles pour l’étude des éco-pathosystèmes et la gestion de la santé ?
- la simulation, visant par exemple à tester des stratégies de contrôle ou des scenarii de changement, et/ou la prédiction des zones ou des périodes à risque de transmission ou de propagation d’agents pathogènes ?
3) Comment mieux intégrer les connaissances expertes et multi-disciplinaires, afin de :
- Mieux cibler les situations et phénomènes d’intérêt pour l’étude d’une question de santé ?
- Guider la caractérisation de ces situations et phénomènes d’intérêt et construire des modèles plausibles des points de vue biologique, écologique, socio-démographique, comportemental, etc. ?
- Guider l’analyse et l’interprétation des données, des indicateurs et des sorties des modèles par les utilisateurs finaux ?
L’ensemble de ces questions sont directement associées à l’enjeu majeur des recherches dans le domaine : faciliter l’appropriation et l’exploitation des données de télédétection, des indicateurs de risque, des sorties des modèles, etc. par les utilisateurs finaux (chercheurs, gestionnaires de santé, grand public, etc.) et participer plus directement à la mise en place de stratégies de prévention et de lutte.
Quelques produits santé Theia
CES Theia concernés
Actualités Theia sur la santé
Applications
ANISETTE | ANalyse Inter-Site : Evaluation de la Télédétection comme ouTil prédictif pour la surveillance et le contrôle de maladies causées par des moustiquEs. (2019-2021)

https://anisette.cirad.fr
L’objectif principal du projet ANISETTE est de mesurer l’interopérabilité des approches développées par les équipes partenaires pour la prédiction des zones favorables au développement des moustiques, par une analyse inter-sites : pour des sites géographiques et des espèces de moustiques différentes.
Les objectifs spécifiques portent sur :
• l’identification des images d’Observation de la Terre les mieux adaptées au développement d’outils prédictifs de dynamiques de populations de moustiques et de la transmission de maladies vectorielles, en termes de résolutions spatiales, temporelles et spectrales, ainsi que de leurs complémentarités. L’analyse portera en particulier sur le potentiel des séries temporelles d’images (Sentinel-2, MODIS) et leur complémentarité avec d’autres types de capteurs (radar – Sentinel-1, thermique – Landsat8) et images optiques à plus haute résolution spatiale (SPOT 6/7, Pleiades).
• l’analyse du potentiel et des limites de différentes approches de modélisation (modèles basés sur les données, sur les connaissances, sur les processus) ;
• la diffusion et le transfert des méthodes validées.
Nous proposons comme modèle d’étude les moustiques du genre Aedes (vecteurs de la dengue, de la fièvre de la Vallée du Rift) et Anopheles (vecteurs du paludisme).
Partenaires : Cirad | Tetis |Astre | IRD | espaceDEV | CNRS | IDEES | Institut Pasteur | CNES
Financement : CNES
Publications : Dans le numéro spécial de Remote sensing « Remote Sensing for Health: from Fine-Scale Investigations towards Early-Warning Systems » (Editeur : V. Herbreteau)
Tran A, Fall AG, Biteye B, Ciss M, Gimonneau G, Castets M, Talla Seck M, Chevalier V. 2019. Spatial modeling of mosquito vectors for rift valley fever virus in northern Senegal: Integrating satellite-derived meteorological estimates in population dynamics models. Remote Sensing, 11 (9) (1024) : 24 p.
Sentinel-2 for Malaria surveillance (S2-Malaria) (08/2017-07/2020)
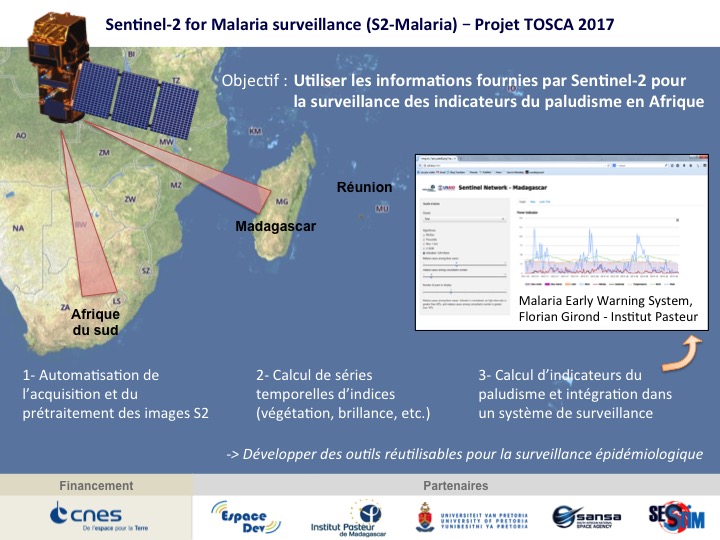
L’objectif principal du projet S2-Malaria est d’utiliser les informations fournies par les satellites Sentinel-2 pour la surveillance du paludisme en Afrique. Les données issues de l’acquisition et du traitement des images Sentinel-2 par le projet seront : 1) utilisées comme source d’information environnementale dans un système de surveillance du paludisme et 2) mises à disposition sous forme de séries temporelles d’indices spectraux simples sur les sites d’étude pour les utilisateurs finaux (initialement à Madagascar et en Afrique du sud). Le projet répond à trois sous-objectifs méthodologiques :
- Adapter au projet les chaînes existantes pour l’acquisition et le prétraitement des images Sentinel-2. La chaîne sen2chain a ainsi été produite pour faciliter le téléchargement des images et le traitement du niveau L1C au niveau L2A, la production d’indices et le calcul des séries temporelles (https://framagit.org/jebins/sen2chain) ;
- Intégrer la chaîne d’acquisition puis le calcul des indices dans un système de surveillance ;
- Tester les indices spectraux déjà utilisés (à partir d’autres capteurs) et créer d’autres indices pertinents pour la surveillance du paludisme (en utilisant la richesse spectrale de Sentinel-2).
A plus long terme, l’objectif est de rendre ces produits d’images facilement utilisables pour la surveillance épidémiologique mais aussi de démultiplier les usages où les séries temporelles à haute résolution spatiale sont nécessaires.
Localisation : Madagascar, Afrique du Sud
Partenaires : UMR Espace-Dev – IRD, Institut Pasteur de Madagascar, UMR SESSTIM – IRD, University of Pretoria, CNES
Financement : CNES TOSCA
Référence : Herbreteau Vincent, Révillion Christophe, Wolff Charlotte, Surveiller le paludisme à Madagascar grâce aux satellites, [IGN Mag] 88 (2017).
Site Web : (Chaîne sen2chain pour le traitement de séries d’images Sentinel-2) https://framagit.org/jebins/sen2chain
ECOMORE II | ECOnomic development, ECOsystem MOdifications, and emerging infectious diseases Risk Evaluation (2018-2020)

Site Web : http://www.ecomore.org/
Le projet ECOMORE 2 vise à étudier l’impact des modifications des écosystèmes sur la santé des populations sous l’effet de l’activité humaine (urbanisation, intensification des techniques agricoles, utilisation des sols, mouvements des populations) et des changements climatiques. Il est financé par l’AFD et s’inscrit dans les fortes préoccupations au niveau international et régional soulevées par la COP21. Un volet « climat-environnement » du projet ECOMORE2 propose de mettre en place un service climatique pour cartographier le risque de transmission de la dengue et de la leptospirose dans les pays partenaires, qui ont connu plusieurs épidémies au cours de la dernière décennie. L’objectif est d’estimer l’évolution de ces risques dans le cadre du changement climatique, à partir des données multimodèles climatiques du GIEC (Groupe intergouvernemental sur l’évolution du climat), pour différents scénarios d’émissions afin de déterminer si la dengue, la leptospirose et les vecteurs peuvent se répandre hors de leurs frontières actuelles. Localement, le volet « climat-environnement » visera aussi à analyser spatialement les enquêtes de surveillance épidémiologiques et entomologiques réalisées dans chaque pays.
Localisation : Cambodge, Laos, Myanmar, Vietnam
Partenaires : UMR Espace-Dev – IRD, UMR LOCEAN – IRD et UMR TETIS – Cirad, pour le volet « climat-environnement » du projet Ecomore 2.
Le projet Ecomore 2 est coordonné par l’Institut Pasteur International. Il réunit l’Institut Pasteur du Cambodge (Phnom Penh), l’Institut Pasteur du Laos (Vientiane), le National Institute of Hygiene and Epidemiology au Vietnam (Hanoï), le National Health Laboratory (Yangon), le Research Institute for Tropical Medicine aux Philippines (Manille) et l’IRD en France, au Cambodge et au Vietnam.
Financement : Agence Française de Développement (AFD)
Projet TEMPO : TElédétection et Modélisation sPatiale de la mObilité animale | Application à l’étude des contacts faune domestique / faune sauvage et du risque de transmission d’agents pathogènes (2018-2021)

Buffles équipés d’un collier GPS @Cirad D. Cornelis
L’objectif principal du projet TEMPO est de modéliser, à partir de données d’Observation de la Terre, l’utilisation du paysage par des populations animales sauvages et domestiques afin de mieux caractériser les contacts et leurs déterminants dans les zones d’interface sauvage/domestique et d’estimer le risque de transmission d’agents pathogènes.
Nous proposons de prendre comme modèle d’étude les contacts entre herbivores domestiques et sauvages à la périphérie des aires protégées en Afrique Australe, une région du monde qui abrite de nombreux parcs nationaux et où les mouvements d’animaux entre les habitats naturels et anthropisés sont fréquemment observés dans les deux directions. Deux types de maladies seront étudiées l’une à transmission directe (la fièvre aphteuse) et la deuxième à transmission indirecte vectorielle (la fièvre de la Vallée du Rift).
Le projet TEMPO s’appuie sur des données de télémétrie, d’enquêtes et d’épidémiologie déjà disponibles (acquises dans le cadre de projets antérieurs), et porte principalement sur le développement de méthodes innovantes en modélisation
Trois volets structurent ce projet : (1) la caractérisation et le suivi par télédétection des déterminants environnementaux de l’occupation de l’espace et des déplacements des animaux sauvages et domestiques ; (2) la modélisation des dynamiques d’occupation de l’espace prenant en compte ces déterminants environnementaux et anthropiques (conduite d’élevage) ; (3) la modélisation du risque de transmission de pathogènes entre populations animales sauvages et domestiques. spatiale pour la simulation de la mobilité animale. Les défis méthodologiques principaux qui seront adressés sont l’assimilation dans les modèles de données d’Observation de la Terre multi-capteurs, et la modélisation de la mobilité à différentes échelles.
Localisation : Zimbabwé, Mozambique
Partenaires : UMR TETIS/CIRAD, UMR ASTRE/CIRAD, UMR MIVEGEC/IRD, Faculty of Veterinary Science/University of Zimbabwe, Faculdade de veterinaria/Universidade Eduardo Mondlane
Financement : i-site MUSE, GEOSUD (appui images)
Site Web : https://tempo.cirad.fr
Projet ARBOCARTO : Modélisation spatiale dynamique des populations d’Aedes albopictus – France métropolitaine et Régions d’Outre-Mer (2018)
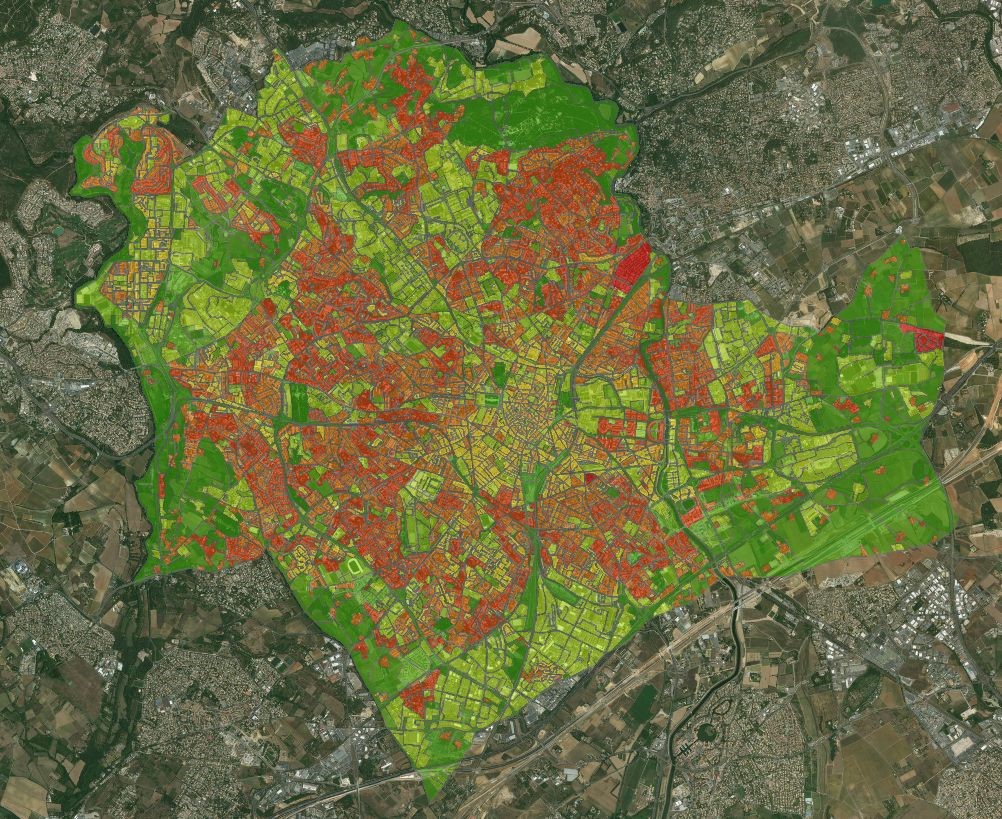
Le moustique ‘tigre’ Aedes albopictus est un des vecteurs des virus de la dengue, du chikungunya, du Zika, et pleinement adaptés aux milieux urbains. Aedes albopictus est présent dans l’Océan Indien (Réunion et Mayotte) et dans de nombreux départements de France métropolitaine, ainsi qu’aux Antilles et en Guyane. La présence concomitante de populations de moustiques vecteurs et d’arbovirus est à l’origine d’épidémies intenses dans les différents territoires outre-mer et constitue un risque important également pour la France hexagonale, où le moustique ‘tigre’ constitue également une forte nuisance dans les régions où il s’est implanté tout récemment.
L’objectif du projet Arbocarto veut développer un outil de cartographie prédictive des densités de populations d’Aedes albopictus à une échelle spatiale adaptée à l’organisation des actions de surveillance et de contrôle menées par les acteurs de la lutte anti-vectorielle dans différents départements français, à partir de données météorologiques (températures et pluviométrie quotidienne) et de télédétection à haute et très haute résolution spatiale.
Bénéficiant de l’expertise du Cnes, il s’inscrit dans la continuité des travaux menés par le CES Risques maladies infectieuses depuis plusieurs années en collaboration avec l’EID-Méditerranée (Tran et al., 2013) et l’Agence de Santé Océan Indien (Tran et al. 2017, Roux et al. 2017).
Localisation : France métropolitaine et Régions d’Outre-Mer
Partenaires : UMR TETIS/CIRAD, UMR Espace-Dev/IRD, Marie Demarchi, EID-Méditerranée, EID-Rhône Alpes, EID-Atlantique, ARS-Occitanie, CNES
Financement : Direction e de la Santé et Agences de Santé Auvergne Rhône Alpes et Nouvelle Aquitaine, GEOSUD (appui images)
Références
- Roux E., Tran A., Herbreteau V., Révillion C., Demarchi M., Mangeas M., Degenne P., Dehecq J.S. 2017. Space-time modelling of mosquito densities : application to Aedes albopictus, vector of viruses, in Reunion Island. GEOMED 2017, International Conference on Spatial Statistics Spatial Epidemiology and Spatial aspects of Public Health. Porto, Portugal, 7-9 September
- Tran A., L’Ambert G., Lacour G., Benoît R., Demarchi M., Cros M., Cailly P., Aubry-Kientz M., Balenghien T., Ezanno P. 2013. A Rainfall- and Temperature-Driven Abundance Model for Aedes albopictus Populations. International Journal of Environmental Research and Public Health, 10 (5) : p. 1698-1719.
- Tran A., Herbreteau V., Demarchi M., Mangeas M., Roux E., Degenne P., Dehecq J.S. 2017. Spatial modeling of mosquito population dynamics : an operational tool for the surveillance of vector-borne diseases. 37th International Symposium on Remote Sensing of Environment (ISRSE-37) : Earth Observation for Development and Adaptation to a Changing World, 8-12 Mai, Tshwane (Afrique du Sud).
TELENipah : Apport de la télémétrie et de la télédétection à la cartographie du risque de transmission du virus Nipah à l’interface environnement, chauves-souris, hommes au Cambodge
Le projet TéléNipah vise à mieux comprendre les contacts entre des chauves-souris et l’Homme pour évaluer les risques d’émergence du virus Nipah au Cambodge.
Le Projet TéléNipah a pour objectif principal de combiner télédétection et télémétrie, à l’étude de l’interface entre Pteropus lylei et l’Homme pour estimer le risque d’émergence du virus Nipah au Cambodge. Si nous savons que le virus circule chez les chauves-souris, rien n’est connu d’une potentielle transmission à l’Homme dont les activités, notamment agricoles, l’amène en contact avec les populations de P. lylei qui forment des colonies à proximité des zones d’habitations humaines, parfois au cœur des villes.
Le projet TéléNipah a 3 objectifs spécifiques :
- la caractérisation et la cartographie des habitats entourant une colonie de P. lylei à partir de données de télédétection,
- la cartographie des zones de contact potentiel avec l’Homme en analysant la sélection de l’habitat de P. lylei à partir des données de télédétection et de télémétrie,
- et la cartographie des zones de risque d’émergence du Nipah à l’échelle du Cambodge.
Localisation | Cambodge.
Partenaires | Institut Pasteur du Cambodge.
Financement | Centre National d’Etudes Spatiales (CNES).
Publication
- Choden K, Ravon S, Epstein JH, Hoem T, Furey N, Gely M, Jolivot A, Hul V, Neung C, Tran A, Cappelle J. Pteropus lylei primarily forages in residential areas in Kandal, Cambodia. Ecol Evol. 2019 Mar 13;9(7):4181-4191. doi: 10.1002/ece3.5046.
Evaluation de la contribution de la télédétection multi-dates et multi-capteurs dans la construction d’indicateur spatialisé du risque de transmission du paludisme en région amazonienne – TéléPal (05/2015-05/2017)
L’objet d’étude est le paludisme qui en 2015 a provoqué le décès de 438 000 personnes à travers le monde. La zone étudiée concerne les rives du fleuve Oyapock, frontière naturelle entre la Guyane française et l’état brésilien d’Amapa, et plus précisément des communes situées de part et d’autre du fleuve : St Georges de l’Oyapock et Camopi en Guyane française et Oiapoque au Brésil. L’objectif du projet est d’exploiter et de combiner des données satellitaires multi-sources, multi-résolutions et multi-temporelles afin de caractériser les niches écologiques des vecteurs (moustiques du genre Anopheles), l’empreinte spatiale des activités humaines, et les interactions homme-vecteur.
Le projet est structuré en quatre tâches :
- Caractériser, à partir de données optique (Landsat 8 à 30 m, Spot 5 à 10 m, Pléiades à 2 m) et radar (Sentinelle 1 à 10 m, TerraSarX à 1 m), les différents milieux favorables à la transmission du paludisme.
- Développer de nouvelles approches d’analyse de paysages afin de mettre en évidence, via la construction d’indicateurs spatialisés de risque et l’exploitation de données entomologiques et épidémiologiques, les interactions et les risques de transmission homme-vecteur dans les villages de la zone transfrontalière.
- Evaluer l’apport des différentes sources de données satellitaires (y compris les satellites altimétriques) dans la caractérisation de l’habitat des vecteurs.
- Valoriser les résultats.
Localisation : zone transfrontalière Guyane française – état brésilien d’Amapa
Partenaires : UMR ESPACE-DEV/IRD, Laboratoire Central d’Epidémiologie d’Amapá (LACEN-AP, Brésil), Institut National de Recherche de l’état d’Amapá (IEPA, Brésil), Laboratoire de Parasitologie/Institut Pasteur de Guyane, Equipe Associé Ecosystèmes Amazoniens et Pathologies Tropicales (EpaT/UG),Laboratoire de Géographie, Environnement et Santé de l’Université de Brasilia (LAGAS/UnB), Observatoire Climat et Santé de la Fondation Oswaldo Cruz (Fiocruz), UMR LETG 6554 CNRS – COSTEL/CNRS.
Financement : Centre National d’Etudes Spatiales (CNES). GEOSUD (Appui Images)
Guyane française – Amapá – Amazonas – Malaria : Site sentinelle transfrontalier de l’Observatoire Climat et Santé – GAPAM-Sentinela (2015-2017)
Les objectifs généraux du projet GAPAM-Sentinela sont de contribuer à la mise en place d’un site sentinelle transfrontalier de l’observatoire brésilien climat et santé (www.climasaude.icict.fiocruz.br), consacré au paludisme dans la zone transfrontalière Guyane Brésil, et d’étudier la transposition des méthodologies, outils et modèles à la tri-frontière Brésil–Colombie–Pérou.
Trois axes de recherche sont considérés : la production de référentiels cartographiques et de couches d’information socio-démographiques et environnementales, en utilisant notamment la géomatique, la télédétection et les enquêtes de terrain ; le développement de méthodes de représentation, de partage et d’intégration de données et informations hétérogènes et multidisciplinaires, au moyen de modèles de données et de méta-données et de la formalisation des connaissances par les ontologies ; la contribution au recueil routinier de l’information spatialisée pour l’actualisation des données et des indicateurs, par la rationalisation des protocoles de collecte et l’exploitation de référentiels cartographiques.
Localisation : zone transfrontalière Guyane française – Brésil
Partenaires : IRD, Institut Pasteur de la Guyane, Service des Centres Délocalisés de Prévention et de Soin (CDPS) du Centre Hospitalier Andrée Rosemon de Cayenne (CHAR), Equipe Associé Ecosystèmes Amazoniens et Pathologies Tropicales (EpaT/UG), Laboratoire Central d’Epidémiologie d’Amapá (LACEN-AP, Brésil), Institut National de Recherche de l’état d’Amapá (IEPA, Brésil), Fondation de Veille Sanitaire de l’état d’Amazonas (FVS-AM, Brésil), Laboratoire de Géographie, Environnement et Santé de l’Université de Brasilia (LAGAS/UnB), Observatoire Climat et Santé de la Fondation Oswaldo Cruz (Fiocruz)
Financement : Programme Franco-Brésilien de recherche et de renforcement des capacités Guyamazon (IRD, CIRAD, Collectivité Territoriale de la Guyane, Ambassade de France au Brésil, Fondations d’appui à la Recherche des états du Maranhão, de l’Amapá et de l’Amazonas)
Observation Spatiale de l’Environnement transfrontalier Guyane -Brésil – OSE-Guyamapá (2012-2014)
Guyamapa est un projet multi-thématique qui a pour vocation de proposer un socle commun de pratiques et d’outils destiné à mettre en place, à terme, un observatoire des patrimoines naturels transfrontaliers au service des territoires et de la coopération régionale. Ce système d’observation de l’environnement à partir de données spatiales et de données thématiques repose sur des méthodes de traitement de l’information co-construites entre acteurs du projet.
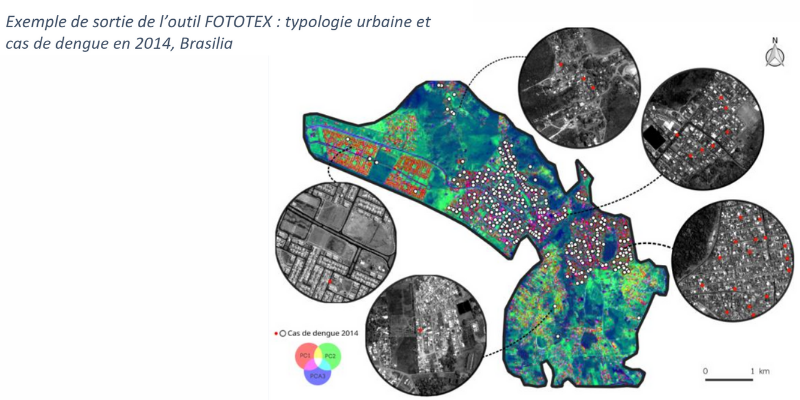
Le groupe de travail « indicateurs environnementaux du risque de transmission du paludisme » a plus particulièrement pour objectif de définir une typologie d’occupation/usage du sol pertinente pour l’étude du risque de transmission de la maladie en milieu amazonien, de construire des indicateurs de risque de transmission et de les spatialiser afin d’obtenir des cartes de risque.
Localisation : zone transfrontalière Guyane française – Brésil
Partenaires de l’Axe Paludisme : IRD, Institut Pasteur de la Guyane, Service des Centres Délocalisés de Prévention et de Soin (CDPS) du Centre Hospitalier Andrée Rosemon de Cayenne (CHAR), Equipe Associé Ecosystèmes Amazoniens et Pathologies Tropicales (EPaT/UG), Laboratoire Central d’Epidémiologie d’Amapá (LACEN-AP, Brésil), Institut National de Recherche de l’état d’Amapá (IEPA, Brésil), Laboratoire de Géographie, Environnement et Santé de l’Université de Brasilia (LAGAS/UnB)
Financement : Programme Opérationnel Amazonie (FEDER-Guyane), IRD, CNES, INPE, CLS
Évaluation de l’impact des conditions environnementales sur la productivité des gîtes larvaires pour une cartographie prédictive du risque vectoriel à La Réunion (2015 – 2016)
Ce projet a comme objectifs :
- De caractériser et de modéliser l’impact des conditions météorologiques sur la productivité des gîtes larvaires d’Aedes albopictus (moustique tigre) à la Réunion ;
- De développer un outil opérationnel d’évaluation spatiale prédictive des densités vectorielles
Il se décline en 3 phases :
- l’analyse de la productivité des gîtes
- le développement d’un modèle spatial du risque vectoriel
- le transfert de compétence à l’Agence Régionale de Santé Océan Indien.
Localisation : Ile de la Réunion
Partenaires : Cirad, IRD, Marie Demarchi (Ing. indépendante)
Financement : Agence Régionale de Santé Océan Indien
Utilisation de l’imagerie MODIS pour cartographier le risque de la fièvre du Nil Occidental en Europe
Le virus du Nil Occidental (ou West Nile virus, noté WNV) est un pathogène transmis par la piqûre d’un moustique infecté, responsable de la fièvre du Nil Occidental (ou West Nile fever, notée WNF). La distribution géographique de cette maladie a été profondément modifiée au cours des dernières décennies, avec l’apparition du WNV pour la première fois sur le continent américain en 1999, et la recrudescence depuis 2010 de cas dans de nombreux pays d’Europe du Sud et de l’Est, alors que le virus circulait auparavant « à bas bruit » en Europe.
Le cycle de transmission du WNV implique un insecte vecteur, un réservoir animal et des hôtes accidentels, le cheval et l’homme. Plusieurs espèces de moustiques et d’oiseaux sauvages peuvent jouer le rôle de vecteurs et de réservoirs.
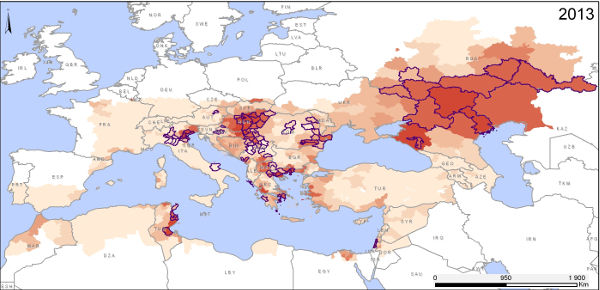
L’objectif d’une étude publiée récemment dans International Journal of Health Geographics était d’étudier la relation entre des variables environnementales et l’occurrence de foyers dus au WNV, afin de pouvoir cartographier les zones à risque de cette maladie, à l’échelle européenne.
Les résultats de l’étude mettent en évidence les facteurs de risque suivants :
- des anomalies positives d’un indice d’eau, calculé à partir d’images MODIS pour le mois de juin,
- des anomalies positives de température au mois de juillet,
- la présence de zones humides,
- la présence de couloirs de migration aviaire,
- l’occurrence de foyers de WNV l’année précédente.
Les modèles prédictifs élaborés à partir des données épidémiologiques reportées entre 2002 et 2011, ont été validés avec les données des épidémies de WNF observées en 2012 et 2013, démontrant la capacité du modèle à prédire les zones à risque d’occurrence de cas de WNF d’une année sur l’autre. De manière générale, cette étude contribue à mieux comprendre les déterminants environnementaux et climatiques de la transmission du virus WN en Europe, et mettent en évidence le rôle de la télédétection spatiale dans la mise en place de systèmes de surveillance en santé publique incluant un suivi environnemental.
Pour en savoir plus :
Tran A., Sudre B., Paz S., Massimiliano R., Desbrosse A., Chevalier V., Semenza J., 2014. Environmental predictors of West Nile fever risk in Europe. International Journal of Health Geographics 13: 26. URL : http://www.ij-healthgeographics.com/content/13/1/26

Annelise Tran
Cirad | Tetis
@A.Tran
Contributions
Utilisation de l’imagerie SPOT pour planifier les études de terrain : application à l’étude de la bio-écologie des vecteurs du paludisme en Guyane française
Le paludisme est une maladie endémique en France, plus précisément dans les départements de Mayotte et de Guyane. Dans ce dernier, 3450 personnes en moyenne, sur un total de 230 000 à 300 000 habitants, étaient touchées par la maladie dans les années 2000. Ce nombre a significativement diminué depuis 2010 pour passer en dessous des 1000 cas en 2012, mais la transmission y est encore une des plus élevées des Amériques et ses déterminants restent encore méconnus.
En particulier, les espèces de moustique du genre Anopheles, dont certaines sont responsables de la transmission à l’homme du parasite à l’origine de la maladie (Plasmodium), doivent régulièrement faire l’objet d’un recensement et de la caractérisation de leur habitat.

Ce besoin a conduit à mener une étude(1) sur la bio-écologie des anophèles en Guyane. Le village de Cacao a été choisi afin de capturer des moustiques adultes et de caractériser leur habitat. En effet, des relevés antérieurs y avaient mis en évidence la présence d’une grande diversité d’espèces d’anophèles, il est facile d’accès et présente une grande hétérogénéité de faciès paysagers. Or, la technique de capture des moustiques, par appât humain, est coûteuse en temps et en main d’oeuvre, et de fait ne permet pas de bénéficier d’un grand nombre de sites de capture. Ainsi, dans la présente étude, ce nombre a été fixé à douze au regard des moyens disponibles.
Dans ce contexte, une étude, publiée dans la revue BMC Ecology, avait pour objectif de définir et de mettre en application une méthode permettant de faire le choix des sites de capture de la manière la plus objective possible, en veillant à ce qu’ils correspondent à des contextes environnementaux, d’une part, significativement différents les uns des autres, et d’autre part, typiques de la région.
La méthode proposée a tout d’abord consisté a réaliser une caractérisation environnementale poussée de la zone d’étude, des points de vue de l’hydrographie, de l’anthropisation, de la topographie et de l’occupation du sol, et ce au moyen de diverses sources de données : cartes et photographies aériennes de l’Institut National Géographique, modèle numérique d’élévation de la NASA (SRTM), images satellitaires SPOT5 fournies par la station de réception SEAS-Guyane.
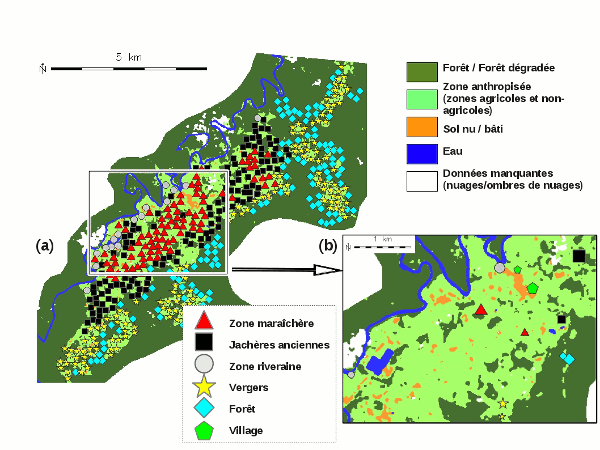
La deuxième étape a permis d’identifier et de caractériser six contextes paysagers distincts et typiques selon ces différents points de vue : le village, les rives de la rivière Comté, les zones maraichères de la plaine, les zones de jachères anciennes, les vergers sur les pentes et les hauteurs des collines, la forêt dense. Enfin, le choix de deux sites de capture dans chacun de ces faciès a été réalisé en tenant des compte des contraintes d’accessibilité du terrain.
Les résultats des captures confirment la présence d’une grande diversité d’espèces d’Anopheles (10 espèces capturées au total), dont le vecteur principal du paludisme en Amazonie (An. darlingi) et 5 espèces vectrices secondaires. Ils démontrent également que, même dans une zone relativement réduite (d’environ 15 km sur 5km) telle que celle étudiée à Cacao, les espèces d’anophèles peuvent être structurées géographiquement et que l’occupation du sol, caractérisée par télédétection, contribue significativement à expliquer leur répartition.
Pour en savoir plus :
Roux E., Gaborit P., Romaña C. A., Girod R., Dessay N., Dusfour I., 2013. Objective sampling design in a highly heterogeneous landscape – characterizing environmental determinants of malaria vector distribution in French Guiana, in the Amazonian region. BMC Ecology 2013, 13:45. URL : http://link.springer.com/article/10.1186/1472-6785-13-45
UMR228 Espace pour le Développement (Espace-Dev): http://www.espace-dev.fr/
Institut Pasteur de la Guyane : http://www.pasteur-cayenne.fr

Emmanuel Roux
IRD | UMR Espace-Dev
@E.Roux

Isabelle Dusfour
Institut Pasteur
idusfour@pasteur-cayenne.fr
(1) Étude réalisée dans le cadre du programme de recherche Bioécologie des anophèles vecteurs du paludisme à Cacao, Guyane française : vers l’évaluation du risque d’exposition au paludisme et l’amélioration de la lutte antivectorielle, subventionné par le Secrétariat d’Etat à l’Outre-Mer et portée par l’Institut Pasteur de la Guyane en collaboration avec l’Unité Mixte de Recherche Espace pour le Développement (Espace-Dev) (IRD, UAG, UM2, UR).
Thèses
- Modélisation de la dynamique du paludisme à Madagascar Hanitriniaina Felana Angella IHANTAMALALA | Université de La Réunion, UMR Espace-Dev, Institut Pasteur de Madagascar, 2017.
- Mise en place d’un système d’information géographique pour la détection précoce et la prédiction des épidémies de paludisme à Madagascar Florian Girond | Université de La Réunion, UMR Espace-Dev, Institut Pasteur de Madagascar, 2017
- Modélisation des relations entre occupation–usage du sol et distribution spatiale du paludisme par télédétection optique et radar. Application à un environnement en évolution : région transfrontalière Guyane française – Brésil
Zhichao Li | Décembre 2016, Université de Montpellier - Télédétection et paludisme en Guyane : déterminants environnementaux de la distribution et de la densité des moustiques anophèles
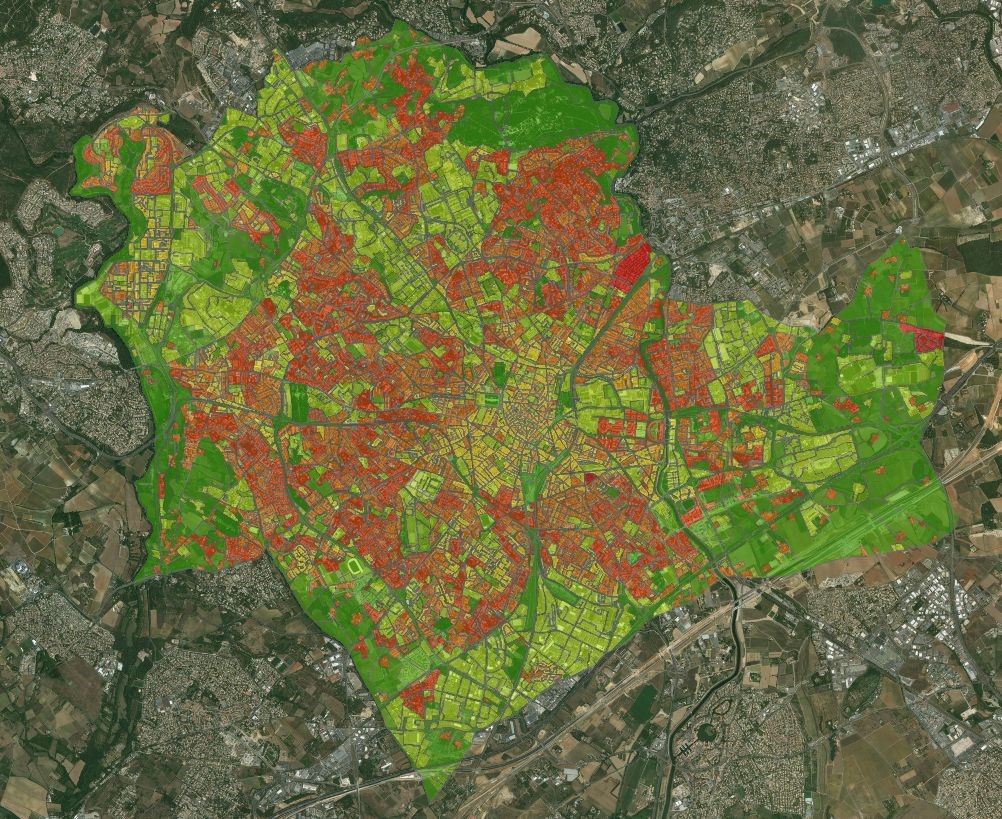
Antoine Adde | Novembre 2016, Université des Antilles - Modélisation à base d’agents des risques vectoriels en milieux urbains : exemple d’Aedes aegypti, vecteur de la dengue à Delhi (Inde)
Somsakun Maneerat | 2016 | Université de Rouen - Segmentations urbaines et disparités de santé dans une ville moyenne africaine : du paludisme aux états nutritionnels à Bobo-Dioulasso (Burkina Faso)
Daouda Kassié | 2015 | Université Paris 10. - Modélisation multi-échelle de la dynamique spatiale de la dengue : application à la Nouvelle Calédonie et à la région Pacifique
Magali Teurlai | Décembre 2014, Université Montpellier 2 - Extraction de relations spatio-temporelles à partir des données environnementales et de la santé
Hugo Alatrista-Salas | 2013 | Université Montpellier 2 - Modélisation du risque d’exposition aux moustiques vecteurs de Plasmodium spp. dans un contexte de lutte anti-vectorielle
Nicolas Moiroux | 2012 | Université Montpellier 2 - Caractérisation des zones et périodes à risque de la Fièvre de la Vallée du Rift au Sénégal par télédétection et modélisation éco-épidémiologique
Valérie Soti | 2011| Université Montpellier 2 - Epidémiologie du paludisme et environnement : étude de deux populations Amérindiennes de l’est et de l’ouest Guyanais
Aurélia Stefani | Décembre 2011 | Université des Antilles et de la Guyane - Utilisation de données d’observation de la terre par satellite pour l’évaluation des densités vectorielles et de la transmission du paludisme
Vanessa Machault | 2010 | Université Aix Marseille 2 - Le risque trypanosomien dans le bassin du Mouhoun au Burkina Faso : approches paysagères
Laure Guerrini | 2009 | Université Montpellier 3
Publications
Adde A., Roux E., Mangeas M., Dessay N., Nacher M., Dusfour I, Girod R. Briolant S. 2016. Dynamical Mapping of Anopheles darlingi Densities in a Residual Malaria Transmission Area of French Guiana by Using Remote Sensing and Meteorological Data. PLoS ONE, Public Library of Science, 11 (10)
Adde A., Dusfour I., Roux E., Girod R., Briolant S. 2016. Anopheles fauna of coastal Cayenne, French Guiana: modelling and mapping of species presence using remotely sensed land cover data. Mem Inst Oswaldo Cruz, 2016, 111 (12) pp.1 – 7
Amaral T.B., Gond V., Tran A.. 2016. Mapping the likelihood of foot-and-mouth disease introduction along the border between Brazil and Paraguay = Mapeamento do risco de introdução da febre aftosa na fronteira do Brasil com o Paraguai. Pesquisa Agropecuária Brasileira, 51 (5) : p. 661-670.
Blasdell K.R., Morand S., Henttonen H., Tran A., Buchy P.. 2016. Hantavirus seropositivity in rodents in relation to habitat heterogeneity in human-shaped landscapes of Southeast Asia. Spatial and Spatio-Temporal Epidemiology, 17 : p. 27-35.
Catry T., Li Z., Roux E., Herbreteau V., Révillion C., & Dessay N. 2016 | Fusion of SAR and Optical Imagery for Studying the Eco-Epidemiology of Vector-Borne Diseases in Tropical Countries. In Living Planet Symposium (Vol. 740, p. 8).
Catry T., Pottier A., Marti R., Li Z., Roux E., Herbreteau V., Mangeas M., Demagistri L., Gurgel H. et Dessay N. 2018 | Apports de la combinaison d’images satellites optique et RADAR dans l’étude des maladies à transmission vectorielle : cas du paludisme à la frontière Guyane française – Brésil, in Confins. https://journals.openedition.org/confins/15027
Della Rossa P., Tantrakarnapa K., Sutdan D., Kasetsinsombat K., Cosson J.F., Supputamongkol Y., Chaisiri K., Tran A., Supputamongkol S., Binot A., Lajaunie C., Morand S.. 2016 | Environmental factors and public health policy associated with human and rodent infection by leptospirosis: a land cover-based study in Nan province, Thailand. Epidemiology and Infection, 144 (7) : p. 1550-1562.
Girond F, Randrianasolo L, Randriamampionona L, Rakotomanana F, Randrianarivelojosia M, Ratsitorahina M, Brou T.Y., Herbreteau V., Mangeas M., Zigiumugabe S., Hedje J., Rogier C., Piola P., 2017 | Analysing trends and forecasting malaria epidemics in madagascar using a sentinel surveillance network: A web-based application. Malaria Journal 16:72.
Hammami P., Tran A., Kemp A., Tshikae P., Kgori P.M., Chevalier V., Paweska J., Jori F.. 2016 | Rift Valley fever vector diversity and impact of meteorological and environmental factors on Culex pipiens dynamics in the Okavango Delta, Botswana. Parasites and Vectors, 9 (434) : 17 p.
Herbreteau V., Révillion C., Trimaille E.. GeoHealth and QuickOSM, Two QGIS Plugins for Health Applications. In : Baghdadi N. (ed.), Mallet C. (ed.) Zribi M. QGIS and Generic Tools Volume 1 – QGIS in Remote Sensing. London: ISTE, 2018, (1), p. 257-286. (Earth Systems – Environmental Sciences: QGIS in Remote Sensing SET; 1). ISBN 978-1-78630-187-1
Herbreteau V. , Kassié D. , Roux E., Marti R., Catry T., Attoumane A., Révillion C., Commins J., Dessay N., Mangeas M. et Tran A. |Observer la Terre pour appréhender spatialement les inégalités de santé : regard historique et prospectif sur l’utilisation de la télédétection dans le domaine de la santé, in Confins 2018. https://journals.openedition.org/confins/15362
Ihantamalala F.A., Rakotoarimanana F.M.J., Ramiadantsoa T., Rakotondramanga J.M., Pennober G., Rakotomanana F., Cauchemez S., Metcalf C.J.E., Herbreteau V., Wesolowski A., 2018 | Spatial and temporal dynamics of malaria in Madagascar. Malaria Journal, 17, 58.
Li Z., Catry T., Dessay N., Roux E., Mahé E., & Seyler F. 2016 | Multi-sensor data fusion for identifying malaria environmental features. In IEEE International Geoscience and Remote Sensing Symposium (IGARSS), 2016 (pp. 2529-2532)
Li Z., Catry T., Dessay N., Roux E., & Seyler F. 2016 | Mapping soil typologies using geomorphologic features extracted from dem and SAR data: A environmental factor affecting malaria transmission in the Amazon. In IEEE International Geoscience and Remote Sensing Symposium (IGARSS), 2016 (pp. 3140-3143).
Li Z., Roux E., Dessay N., Girod R., Stefani A., Nacher M, Moiret A., Seyler F. 2016. Mapping a Knowledge-Based Malaria Hazard Index Related to Landscape Using Remote Sensing: Application to the Cross-Border Area between French Guiana and Brazil. Remote Sensing, MDPI, 8 (4): 22 p.
Moua Y., Roux E., Girod R., Dusfour I., De Thoisy B., Seyler F., Briolant S. 2016. Distribution of the Habitat Suitability of the Main Malaria Vector in French Guiana Using Maximum Entropy Modeling. Journal of Medical Entomology, Entomological Society of America, dec. 2016: 16 p.
Olive M.M., Chevalier V., Grosbois V., Tran A., Andriamandimby S.F., Durand B., Ravalohery J.P., Andriamamonjy S., Rakotomanana F., Rogier C., Héraud J.M.. 2016. Integrated analysis of environment, cattle and human serological data: Risks and mechanisms of transmission of rift valley fever in Madagascar. PLoS Neglected Tropical Diseases, 10 (7) : e0004827 (17 p.).
Randrianaivo H., Bertaut-Nativel B., André M,. Irabe M., Robillard PY., Boumahni B., Mangeas M., Roux E., Yao Brou T., Gérardin P., Filleul L., Herbreteau V., 2017. Mise en place d’une surveillance spatialisée des malformations congénitales à La Réunion : choix méthodologiques. Bull Epidémiol Hebd. (2):38-44.
Semenza J.C., Tran A., Espinosa L., Sudre B., Domanovic D., Paz S.. 2016. Climate change projections of West Nile virus infections in Europe: Implications for blood safety practices. Environmental Health, 15 (28) (suppl. 1. Healthy-Polis: Challenges and Opportunities for Urban Environmental Health and Sustainability) : 12 p..
http://dx.doi.org/10.1186/s12940-016-0105-4
Soti V., Tran A., Goebel F.R.. 2016. Potential of remote-sensing images to study the effect of natural vegetation on the spatial distribution of greyback canegrub, Dermolepida albohirtum, in Australia. In : Allsop Peter G. (ed.). 29th Congress of the International Society of Sugar Cane Technologists: abstracts book. Chiang Mai : Thailand Society of Sugar Cane Technologists, p. 120-121. ISSCT Congress. 29, 2016-12-05/2016-12-08, Chiang Mai (Thaïlande).
Tran A., Trevennec C., Lutwama J., Sserugga J., Gély M., Pittiglio C., Pinto J., Chevalier V.. 2016. Development and assessment of a geographic knowledge-based model for mapping suitable areas for Rift Valley fever transmission in Eastern Africa. PLoS Neglected Tropical Diseases, 10 (9) : e0004999 (20 p.).
Tran A., Kassié D., Herbreteau V. 2016. Applications of Remote Sensing to the Epidemiology of Infectious Diseases: Some Examples. In: Land Surface Remote Sensing: Environment and Risks, Baghdadi N. & Zribi M. (Eds). ISTE Press – Elsevier. 384 p.